英国牛津大学糖尿病中心、ACE联合主席Rury Holman教授介绍了ACE研究的设计和管理。Holman教授直言,作为一项多中心、随机、双盲、前瞻性的心血管终点试验
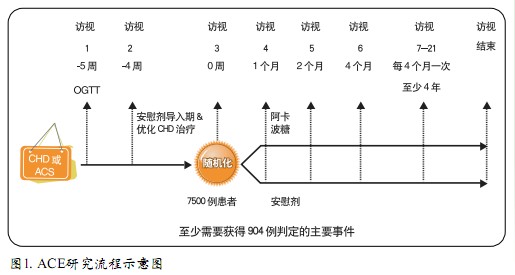
 英国牛津大学糖尿病中心、ACE联合主席Rury Holman教授介绍了ACE研究的设计和管理。Holman教授直言,作为一项多中心、随机、双盲、前瞻性的心血管终点试验,ACE研究对中国来说是个挑战,对牛津大学糖尿病中心也是个挑战。ACE研究在中国大陆和香港开展,目前已经开始招募患者,预计在150家中心入选约7500例患者,至少随访4年(图1),试验结果有望于2014年揭晓。ACE研究由全球享有盛誉的牛津大学糖尿病研究中心组织协调,该中心具有30年的开展多中心研究的经验,曾进行著名的DREAM和UKDPS等研究;由拜耳医药保健公司提供观察药物并资助本研究;指导委员会则由全球糖尿病领域和心血管领域的知名专家组成,其中一半以上的专家来自中国大陆和香港,Rury Holman教授、胡大一教授、潘长玉教授共同担任联合主席,陈家伦教授担任名誉顾问。ACE研究拥有独立的数据安全性监测委员会,由蒙特利尔大学主任Jean-Louis Chiasson教授担任主席,每年2次评价非盲态的安全性数据。
英国牛津大学糖尿病中心、ACE联合主席Rury Holman教授介绍了ACE研究的设计和管理。Holman教授直言,作为一项多中心、随机、双盲、前瞻性的心血管终点试验,ACE研究对中国来说是个挑战,对牛津大学糖尿病中心也是个挑战。ACE研究在中国大陆和香港开展,目前已经开始招募患者,预计在150家中心入选约7500例患者,至少随访4年(图1),试验结果有望于2014年揭晓。ACE研究由全球享有盛誉的牛津大学糖尿病研究中心组织协调,该中心具有30年的开展多中心研究的经验,曾进行著名的DREAM和UKDPS等研究;由拜耳医药保健公司提供观察药物并资助本研究;指导委员会则由全球糖尿病领域和心血管领域的知名专家组成,其中一半以上的专家来自中国大陆和香港,Rury Holman教授、胡大一教授、潘长玉教授共同担任联合主席,陈家伦教授担任名誉顾问。ACE研究拥有独立的数据安全性监测委员会,由蒙特利尔大学主任Jean-Louis Chiasson教授担任主席,每年2次评价非盲态的安全性数据。
研究假设每年的主要事件发生率为3.5%,与安慰剂相比主要复合事件相对降低20%。考虑到两组α为5%,为了获得90%的把握度,ACE研究需要7268例患者,即每组3634例,至少获得904例判定的主要事件。
ACE研究的受试者为合并IGT的心血管疾病患者,主要入选标准为:①男性或女性,年龄≥50岁;②有明确的心血管病史,符合以下三者之一:既往心肌梗死病史、既往不稳定型心绞痛病史、现有的稳定型心绞痛;③OGTT证实为糖耐量减低,即空腹血浆葡萄糖浓度<7.0 mmol/L,同时7.82 mmol/L≤负荷后2小时小时血浆葡萄糖浓度≤11.1 mmol/L;④优化的心血管药物治疗,无介入或手术治疗的计划;⑤签署书面知情同意书。主要排除标准为:①既往有糖尿病病史或妊娠糖尿病病史;②最近三个月内发生过心血管事件;③NYHA分级III或IV级的心力衰竭;④患有严重的肝脏疾病;⑤患有严重的肾功能损害(eGFR<30 ml/min/1.73m2)。鉴于对受试者的限制较少,Holman教授认为入选的患者非常有代表性,这使得该研究结果有望在全世界范围内具有可推广性。
受试者在常规心血管治疗基础上,随机接受阿卡波糖(50 mg,tid)或安慰剂(相似的药片,tid)治疗。药片与餐同服,遵循“小剂量开始,逐渐增量”的给药原则,以提高耐受性。在为期4周的单盲安慰剂导入期,受试者接受优化的冠心病治疗,包括抗血小板治疗,服用他汀类药物(除非禁忌或不能耐受),以及适当地应用ACE抑制剂、β受体阻滞剂和/或抗高血压治疗。
ACE研究的主要终点是随机化后首次发生心血管死亡、心脏停搏复苏、非致死性心梗、非致死性卒中其中之一的时间;次级终点为新发的2型糖尿病(由2次连续的空腹血糖≥7.0 mmol/L和/或负荷后2小时血糖≥11.1 mmol/L证实)、全因死亡及扩展的复合终点(包括心血管死亡、非致死性心梗、非致死性卒中、因心衰或不稳定型心绞痛住院治疗)等;其他结果包括根据ALT水平的变化判断出现非酒精性脂肪肝的患者比例,以及肾功能损害的患者比例,定义为eGFR<60 ml/min/1.73m2或血肌酐水平较基线增高一倍等,另外,如果研究证实阿卡波糖确实能减少心血管疾病风险,研究者将进一步进行卫生经济学评估。
最后,Holman教授强调了合作的重要性,“该研究是一个合作的过程——学术界和企业界之间的合作、心血管科专家和糖尿病科专家之间的合作、试验组成员和调查员之间的合作,更重要的是医生和患者之间的合作。”



 京公网安备 11010502033353号
京公网安备 11010502033353号