近半个世纪以来,综合控制多重危险因素成为心血管疾病(CVD)防治的重心,然而,即使胆固醇、血压、血糖等传统危险因素已得到最佳控制,患者尤其是糖尿病(DM)患者仍面临极高的心血管和微血管剩留风险。以高甘油三酯(TG)、低高密度脂蛋白胆固醇(HDL-C)为特征的致动脉粥样硬化血脂异常是构成剩留风险的主要血脂异常表型。为提高国内广大临床医生对高TG及血管剩留风险的重视程度,推动临床实践中对高TG血症的优化管理,雅培制药于2011年6月16日在北京主办“关注高TG、低HDL-C,降低大、微血管事件风险专家讨论会”,潘长玉教授担任主席,特邀“降低剩留风险行动”(R3i)专家组成员Robert S. Rosenson和Alberto Zambon教授作了精彩报告。
 致动脉粥样硬化血脂异常与大血管剩留风险
致动脉粥样硬化血脂异常与大血管剩留风险
挑战:他汀治疗下心血管剩留风险居高不下
Robert S. Rosenson教授首先强调了针对胆固醇、血压、血糖等传统危险因素的多因素干预是当前指南推荐预防CVD的核心策略,其中他汀降LDL-C治疗已成为CVD防治的基石。TNT、PROVE IT-TIMI 22等研究明确显示,积极他汀治疗下CVD风险已有一定改善。但对于T2DM患者,他汀治疗获益相对较小:胆固醇治疗研究(CTT)协作组对14项冠心病他汀治疗试验的荟萃分析表明,无论对照组(34.9% vs. 24.8%)还是他汀组(29.6% vs. 19.4%),DM患者心血管(CV)剩留风险(主要血管事件发生率)均显著高于非DM患者。
求源:LDL-P——在LDL-C之外
有效控制LDL-C之后仍剩留极高血管风险的本质是什么?Rosenson教授介绍了LDL颗粒(LDL-P)大小和浓度在CV代谢风险中的重要预测作用。Garvey研究表明,随着胰岛素抵抗的加重(直至DM),由高TG导致了一系列脂蛋白颗粒的变化,VLDL颗粒增大,LDL颗粒数量增加,小而密LDL颗粒显著增多,同时HDL颗粒变小。Cromwell的研究进一步证实,T2DM患者LDL-C与LDL-P的变化存在显著的异质性,患者即使LDL-C获得较好控制,但LDL-P浓度仍居高不下,带来很高的剩留风险。
研究表明,在CV代谢高危的个体中,LDL-P提供了与LDL-C不同的风险信息。来自Framingham、女性健康研究等数据的分析显示,LDL-P对未来CV事件的预测价值优于LDL-C。如依据LDL-C和LDL-P水平对Framingham后代研究的受试者进行分层,低LDL-P/无论LDL-C水平,无事件生存率较高;而高LDL-P/ 无论LDL-C水平,无事件生存率较低,充分支持上述结论。
探索:靶向降低LDL-P的策略
基于上述,在LDL-C达标后,降低LDL-P具有十分现实的临床意义。然而,他汀对LDL-P的影响十分有限。COMETS研究表明,代谢综合征(MS)患者接受他汀治疗12周后,LDL-P的降低幅度远低于LDL-C(-30%~-38% vs. -38%~-51%);LDL-P(<1000 nmol/L)的达标率亦远低于LDL-C(<100 mg/dl)(瑞舒伐他汀:80% vs. 27%;阿托伐他汀:59% vs. 19%)。
研究显示,贝特类药物可显著降低LDL-P。Rosenson教授本人一项研究评估了非诺贝特对MS患者空腹和餐后LDL的影响。结果显示,治疗前后LDL-C水平无显著变化;而小而密LDL显著减少(P<0.0001),大LDL显著增加(P<0.0001),同时LDL-P显著降低(P=0.001)。
曙光:ACCORD-Lipid研究带来的启示
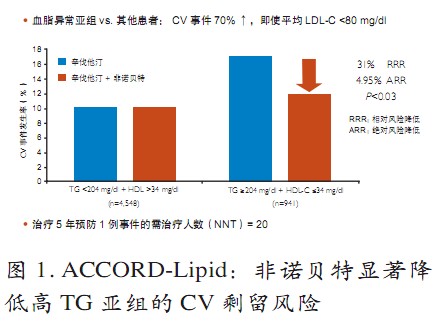
贝特类药物的上述药理作用能否转化为临床硬终点获益?举世瞩目的ACCORD血脂研究虽未能证实在他汀基础上联合贝特可进一步降低一级终点事件的风险,这是由于入选的患者TG的平均水平并不高,只有160 mg/dl左右。但致动脉粥样硬化血脂异常亚组(TG ≥204 mg/dl + HDL-C ≤34 mg/dl)分析结果使降低T2DM患者CVD高剩留风险的探索现出新的曙光:他汀联合非诺贝特显著降低了该组患者主要CV终点的风险达31%,P<0.03(图1)。这一发现与既往FIELD、HHS、BIP、VA-HIT等研究的高TG亚组分析结论一致。
Rosenson教授最后总结,2008年ADA/ACC对有CV代谢风险患者脂蛋白管理的共识声明,强调了该群患者中检测apoB以指导药物治疗的必要性,而LDL-P与apoB相关性极高;对高TG和/或低HDL-C的CV代谢高危患者,他汀仍是一线选择,他汀治疗下仍存在低HDL-C或非HDL-C、尤其apoB升高的患者,应考虑他汀/贝特联合治疗;联合治疗对高TG(≥200 mg/dl)和/或低HDL-C患者可提供额外获益。
 DM微血管剩留风险的管理
DM微血管剩留风险的管理
微血管并发症及其剩留风险——DM患者不能承受之重
Alberto Zambon教授首先回顾了DM微血管并发症导致的巨大医疗负担。当前标准的多因素干预可显著减少DM微血管并发症,但STENO-2研究表明,尽管对T2DM患者施以多重危险因素强化干预,13.3年后仍有51%的患者糖尿病视网膜病变(DR)进展,25%发生糖尿病肾病(DN),55% 糖尿病周围神经病变(DPN)进展。迄今为止的他汀研究,也仅显示可能对降低DN风险有效,而对DR和DPN预防未见获益。微血管剩留风险是DM临床管理所面临的巨大挑战。
非诺贝特具有多重血管效应
研究表明,非诺贝特通过激活PPARa而发挥多重血管效应:促使胆固醇逆向转运从巨噬细胞和动脉粥样硬化病灶流出,减少泡沫细胞形成;下调单核细胞组织因子表达,降低血管致栓性、改善斑块稳定性;降低血管细胞黏附分子-1和炎症细胞因子(IL-6、IFNg 和IL-2)的表达;降低纤维蛋白原和hs-CRP水平;还可减少内皮素-1(ET-1)分泌而缓解血管收缩。这些效应使得非诺贝特具备了微血管保护的药理机制。
微血管剩留风险管理策略
近年来积累的FIELD、ACCORD及ACCORD-EYE等研究证据提示,非诺贝特对降低T2DM微血管风险及剩留风险具有特殊价值。
FIELD试验纳入9795例T2DM患者。随访5年,与安慰剂组相比,非诺贝特组显著降低了需激光治疗的黄斑水肿和增殖性DR的发病率达31%(3.4% vs. 4.9%,P<0.001),尤其对于已诊断DR者,避免首次激光治疗的NNT仅为17例;非诺贝特组降低患者的白蛋白尿进展达14%(P=0.002);虽观察到非诺贝特组血肌酐上升,但停药8周内均自行恢复,较对照组明显降低;且eGFR的降幅低于安慰剂组,可见非诺贝特对肾功能有一定保护作用;FIELD研究还观察到非诺贝特较安慰剂组降低微血管相关的截肢风险达47%(P=0.025)。
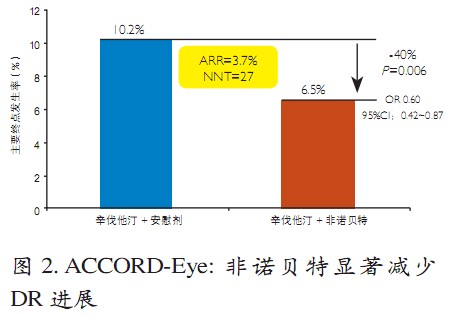
ACCORD试验中,非诺贝特组和安慰剂组终末期肾病或需透析治疗的发生率无差异,且非诺贝特组白蛋白尿的发生率显著下降,同样提示其对肾功能无损害。ACCORD眼亚组纳入2856例患者,经4年随访,非诺贝特组较安慰剂组降低ETDRS分类视网膜病变进展≥3级、以及因DR进展需接受光凝治疗或玻璃体切除术的相对危险达40%(图2),预防1例事件的NNT=27。
Zambon教授总结强调,目前血糖、血压、LDL-C的控制可降低T2DM患者的DR和DN风险,但对DPN无效;他汀预防微血管事件收效甚微,此种治疗下微血管剩留风险仍然极高。非诺贝特显著降低微血管剩留风险,对已有DR、微量白蛋白尿、足溃疡的患者具有重要临床意义。在T2DM患者的管理中,尤其在微血管并发症的风险控制中,贝特类药物应占有重要地位。



 京公网安备 11010502033353号
京公网安备 11010502033353号